Jakarta - Perjuangan BPOM memperoleh pengakuan sebagai otoritas obat dan makanan berkelas dunia melalui status World Health Organization (WHO) Listed Authority (WLA) memasuki tahapan baru. Sesuai roadmap yang telah disepakati antara BPOM dan WHO, Kamis (7/11/2024), WHO dan BPOM menyelenggarakan virtual technical meeting untuk membahas hasil penilaian mandiri pemenuhan persyaratan WLA BPOM. Pertemuan dengan tema “Indonesia Self Benchmarking Feedback & Next Step dalam rangka BPOM menjadi WHO Listed Authority” dibuka dengan brief address Kepala BPOM Taruna Ikrar.
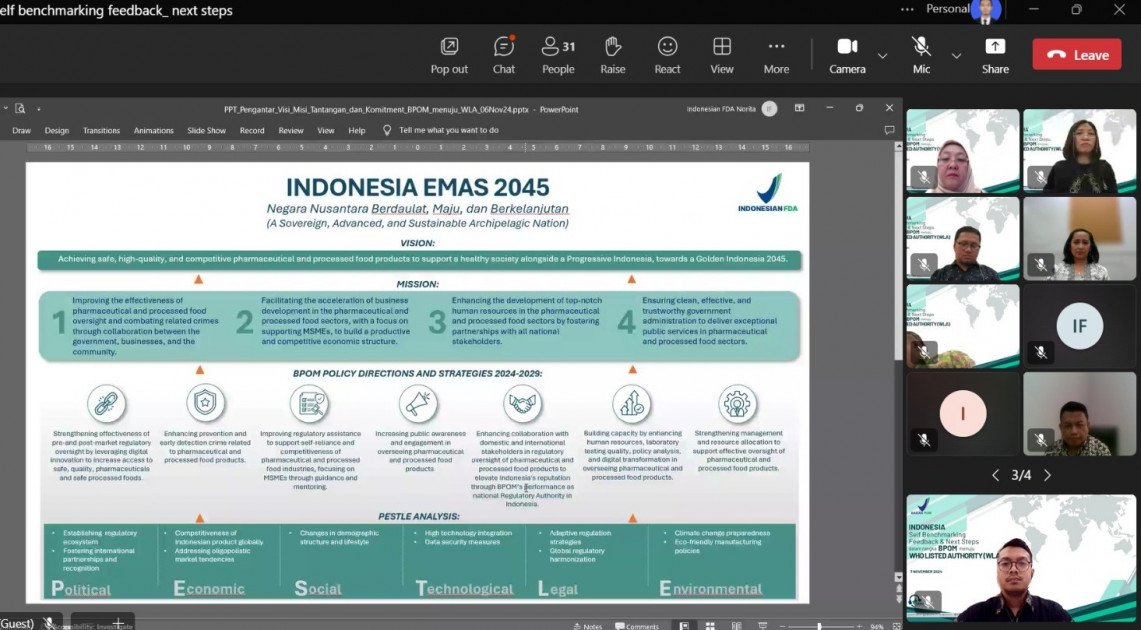
“BPOM memainkan peran penting dalam sistem kesehatan nasional Indonesia, mengawasi proses dari hulu hingga hilir,” tutur Taruna Ikrar dalam brief address-nya. Kepala BPOM menjelaskan bahwa selaras dengan Asta Cita Presiden untuk Indonesia yang Maju dan menuju Indonesia Emas 2045, setidaknya terdapat 4 kontribusi BPOM, yaitu (1) memastikan keamanan dan keselamatan bangsa melalui produk farmasi dan pangan olahan yang berkualitas dan kompetitif; (2) mempromosikan kemandirian nasional dengan memajukan sektor pangan, farmasi, dan sektor terkait; (3) meningkatkan pengembangan sumber daya manusia melalui penyebaran pengetahuan kesehatan masyarakat dan kemajuan teknologi di bidang farmasi dan pangan olahan; dan (4) meningkatkan dukungan regulasi untuk mendukung kemandirian dan daya saing industri farmasi dan pangan olahan, khususnya pada usaha mikro, kecil, dan menengah (UMKM).
“Misi kami lebih dari sekadar menjaga kesehatan masyarakat. Hal ini bertujuan memastikan bahwa setiap orang Indonesia memiliki akses yang konsisten terhadap produk obat berkualitas,” ungkap Taruna Ikrar.
Di hadapan perwakilan WHO, Kepala BPOM menyampaikan selama setahun terakhir, BPOM telah melakukan penilaian mandiri dengan menggunakan WHO Global Benchmarking Tools (WHO GBT) untuk sub-indikator Tingkat Kematangan 4 (maturity level/ML4) dan indikator evaluasi kinerja (PE) WLA di semua 9 fungsi regulasi.
“Kami sepenuhnya siap untuk melanjutkan evaluasi dan berkomitmen untuk kerja sama dan transparansi di setiap tahap,” tegas Kepala BPOM.
Menguatkan pernyataan Kepala BPOM, perwakilan Kedeputian Bidang Pengawasan Obat, Narkotika, Psikotropika, Prekursor, dan Zat Adiktif Rita Endang menyampaikan sejak penilaian benchmarking WHO terakhir terhadap BPOM pada tahun 2018, BPOM telah meningkatkan sistem regulasi secara keseluruhan. Peningkatan sistem tersebut, termasuk proses evaluasi kinerja sebagai bagian dari perbaikan berkelanjutan untuk mempertahankan status sebagai otoritas obat dan makanan dengan tingkat kematangan yang tinggi, sesuai dengan standar internasional dan praktik regulasi yang baik (good regulatory practices/GRP).
Jajaran Kedeputian bidang pengawasan obat, narkotika, psikotropika, prekursor, dan zat adiktif; Kedeputian Bidang Penindakan; Pusat Pengembangan Pengujian Obat dan Makanan Nasional; Pusat Pengembangan Sumber Daya Manusia Pengawasan Obat dan Makanan; Biro Kerja Sama dan Hubungan Masyarakat; serta Biro Hukum dan Organisasi mengikuti pertemuan ini secara luring di Gedung Bhinneka Tunggal Ika BPOM. Hadir secara daring dalam pertemuan penting ini adalah perwakilan Kantor Pusat WHO, yaitu Dr. Razieh Ostad Ali Dehaghi, Dr. Anil Kumar Chawla, Dr. Mhadava Ram Balakrishnan, Dr. Anna Laura Salvati, dan Dr. Engy Elhosary. Turut hadir pula perwakilan WHO South East Asia Region (SEARO) Dr. Adrien Inoublie dan perwakilan WHO Country Office Indonesia Liyana Rakinaturia.
Secara garis besar, hasil reviu WHO terhadap WHO GBT yang disampaikan BPOM menyatakan bahwa BPOM telah bisa menyediakan dokumen yang diperlukan dengan baik dan terstruktur. Pemaparan terkait perubahan sejak WHO GBT Benchmarking pada tahun 2018 sangat transparan, tampak adanya peningkatan yang signifikan.
Pertemuan dilanjutkan dengan diskusi terhadap hasil reviu WHO. Dari reviu ini, WHO memerlukan konfirmasi terhadap fungsi-fungsi yang terdapat pada GBT. Setelah pertemuan ini, masih terdapat beberapa tahapan yang akan dilewati BPOM hingga proses penilaian akhir dan pemberian keputusan.
WLA sendiri mengacu pada otoritas regulasi obat dan vaksin dari negara atau wilayah yang telah memenuhi standar kinerja tertentu yang ditetapkan oleh WHO dalam hal pengawasan produk medis dan farmasi. Otoritas yang terdaftar sebagai WLA dianggap memiliki kapasitas yang cukup untuk mengatur dan mengawasi keamanan serta kualitas produk medis yang beredar di pasar. Hingga Mei 2024, terdapat 34 negara yang sudah masuk dalam WLA, di antaranya Swiss, Singapura, Korea Selatan, Amerika Serikat, Belanda, Denmark, Irlandia, Jerman, dan Prancis.
Untuk mendapatkan status WLA, otoritas regulasi di suatu negara harus melalui proses evaluasi yang mencakup penilaian kinerja yang ketat dalam berbagai aspek, mulai dari pengawasan dan pendaftaran produk medis hingga kemampuan untuk mengelola sistem regulasi secara keseluruhan. Untuk proses evaluasi/audit WLA, WHO biasanya menggunakan GBT, suatu alat untuk menilai kinerja sistem regulasi nasional dan memberikan arahan untuk peningkatan lebih lanjut.
Jika BPOM berhasil mendapatkan status WLA, selain mendapat pengakuan internasional atas kemampuannya dalam mengawasi dan mengatur produk medis, produk obat dalam hal ini vaksin dari Indonesia akan lebih mudah diterima di pasar internasional karena negara tersebut dianggap memiliki sistem pengawasan yang andal dan efisien. Proses menuju WLA sendiri telah membantu BPOM dalam meningkatkan kapasitas teknis dan operasional memperkuat pengawasan di tingkat nasional. (HM-Nelly)
Biro Kerja Sama dan Hubungan Masyarakat